
COVID-19 persistente (“Long COVID”): un estudio multicéntrico en Brasil .
Dra. Ana Paula Bandeira Barboza
Depto. de Moléstias e Parasitárias, Universidad de São Paulo. Brasil.
Brasil fue uno de los países más afectados por la pandemia del SARS-CoV-2.1 En un estudio observacional multicéntrico realizado en San Pablo y Río de Janeiro, se evaluó la prevalencia de COVID-19 persistente, definida por la prolongación de los síntomas más allá de las 4 semanas de la infección aguda, y los factores de riesgo y de protección asociados.
El análisis incluyó 1907 pacientes con COVID-19 entre el 2020 y el 2022. Del total, 104 presentaron infecciones graves con internación. El 52% de la cohorte había recibido dos vacunas y un refuerzo, y 281 pacientes no estaban vacunados.
En el estudio, se identificó una prevalencia de COVID-19 persistente del 67%. Los principales síntomas reportados fueron fatiga (60%), problemas de concentración (55%), pérdida de memoria (45%), artralgias/mialgias (31%).
El sexo femenino, las comorbilidades, la gravedad de la infección y las reinfecciones fueron factores de riesgo para el desarrollo de COVID-19 persistente (ver Cuadro 1).2 Por el contrario, las inmunizaciones fueron factores protectores.
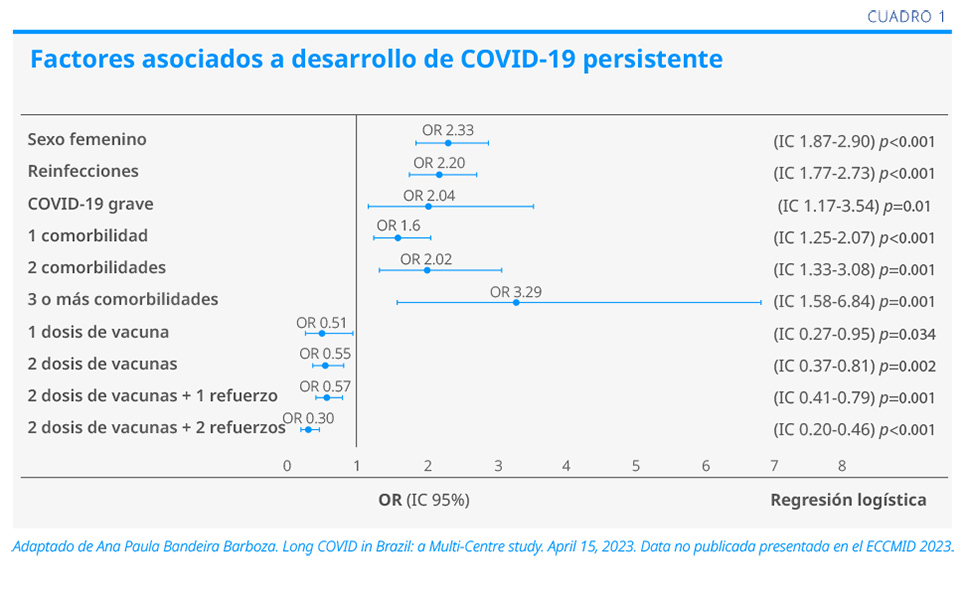
Conclusiones
• La prevalencia de COVID-19 persistente fue alta en las poblaciones estudiadas de Brasil.
• En el sexo femenino, las reinfecciones, las comorbilidades y la infección severa fueron factores de riesgo para el desarrollo de COVID-19 persistente.
• Las inmunizaciones redujeron el riesgo de COVID-19 persistente.
Referencias
1. World Health Organization. Brazil: WHO Coronavirus Disease (COVID-19) Dashboard [Internet]. World Health Organization. Citada el 15 de abril de 2023. Disponible en https://covid19.who.int/region/amro/country/br
2. Bandeira Barboza AP, et al. Long COVID in Brazil: a multi-centre study. April 15, 2023. Data no publicada presentada en el ECCMID 2023.
Fenotipos clínicos de enfermedad aguda leve y su asociación con secuelas a largo plazo: el estudio COVID-HOME
Dra. Adriana Tami
Departamento de Microbiología Médica y Prevención de Infecciones
Centro Médico Universitario
Groningen, Países Bajos.
La finalidad de este estudio fue identificar fenotipos clínicos de enfermedad leve por COVID-19, y determinar las asociaciones entre estos fenotipos y el desarrollo de secuelas a largo plazo (COVID prolongado). Para esto, se realizó en Países Bajos el estudio COVID-HOME,1 estudio prospectivo longitudinal, que incluyó pacientes con infección por COVID-19 que no requerían hospitalización y sus convivientes. Se realizaron visitas en el domicilio a las 48 horas luego del diagnóstico y semanalmente durante 7, 14 y 21 días para obtener información clínica, muestras de sangre, hisopados nasofaríngeos, y muestras de orina, materia fecal, semen y secreción vaginal para testeo de SARS-CoV-2 por PCR y cultivo viral. Luego se realizó un seguimiento a los 3, 6, 12 y 18 meses posinfección. Se incluyeron 256 pacientes y se describieron 3 fenotipos clínicos en pacientes con enfermedad leve. Estos fenotipos difieren significativamente entre sí en edad, sexo, resultados de laboratorio y síntomas reportados (ver Cuadro 2).

Conclusiones
• Se describieron 3 fenotipos clínicos en pacientes con enfermedad leve
• El fenotipo B se asoció significativamente al desarrollo de COVID prolongado
Referencias
1. Tami A., et al. Clinical phenotypes of COVID-19 mild acute disease and their association to long-term sequelae. The COVID-HOME study. April 15, 2023. Data no publicada presentada en el ECCMID 2023.
Impacto del COVID-19 prolongado en la calidad de vida: evaluación funcional de las secuelas a largo plazo en el estudio europeo ORCHESTRA
Dra. Elisa Gentilotti
Departamento de Diagnóstico y Salud Pública
Universidad de Verona, Italia
Un porcentaje de los pacientes que presentaron COVID-19 desarrollaron síntomas persistentes que no pueden explicarse por otra causa.1 El estudio prospectivo ORCHESTRA evaluó las secuelas a largo plazo del COVID-19 e incluyó pacientes de 56 centros asistenciales de 6 países. Utilizó una encuesta de calidad de vida con 36 variables evaluadas en diferentes momentos.2 A continuación, se presenta el análisis del mes 12 de seguimiento. Las variables fueron agrupadas en físicas y mentales. Se incluyeron los aspectos socioeconómicos.
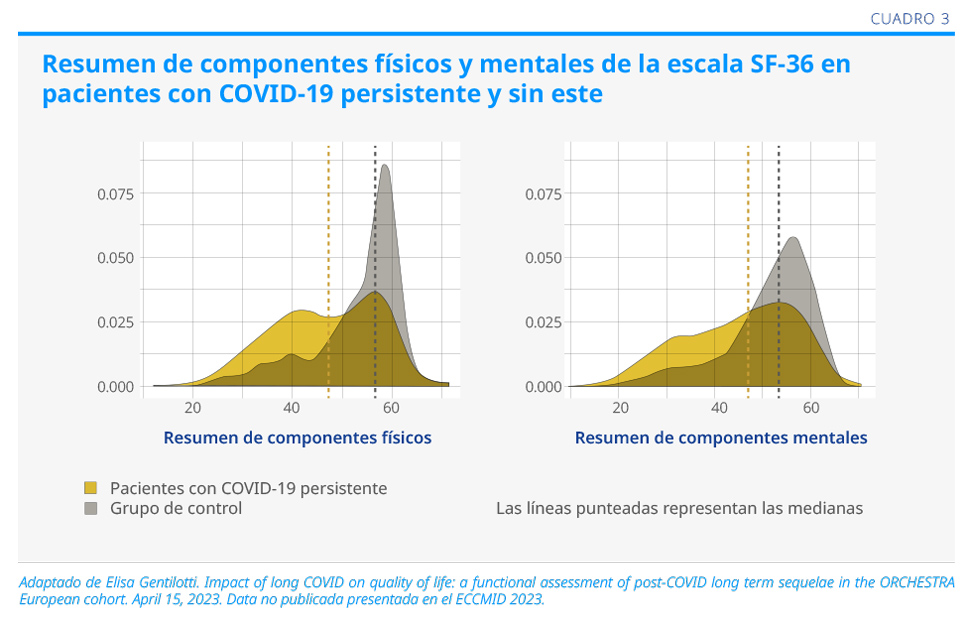
En el estudio participaron 1273 pacientes. La prevalencia del COVID-19 persistente fue del 49%. Los pacientes con al menos un síntoma tuvieron menores puntajes de calidad de vida en los aspectos físicos (47.67% vs. 57.32%, p<0.001) y mentales (46.77% vs. 54.22%, p<0.001), comparados con aquellos que no desarrollaron síntomas (ver Cuadro 3).2
La inmunización fue un factor de protección para el desarrollo de síntomas físicos.
Conclusiones
• Debido a la magnitud de la pandemia, es esperable un incremento de las demandas para atender las complicaciones a largo plazo del COVID-19.1
• El COVID-19 persistente es una patología compleja con impacto en la calidad de vida de las personas e implicancias socioeconómicas.2
Referencias
1. Soriano JB, et al. WHO Clinical Case Definition Working Group on Post-COVID-19 Condition. A clinical case definition of post-COVID-19 condition
by a Delphi consensus. Lancet Infect Dis. 2022 Apr;22(4):e102-e107.
2. Gentilotti E, et al. Impact of long COVID on quality of life: a functional assessment of post-COVID long term sequelae in the ORCHESTRA European cohort. April 15, 2023. Data no publicada presentada en el ECCMID 2023.
Características de long COVID en una cohorte de pacientes de la región de Campania, Italia: un estudio de cohorte prospectivo
Dr. Francesco Carusso
División de Enfermedades Infecciosas de la Universidad de Campania, Italia
Se puede llamar long COVID a la imposibilidad de volver al estado de salud previo luego de la fase aguda de enfermedad por COVID-191. La OMS lo define como la persistencia o el desarrollo de nuevos síntomas clínicos luego de 3 meses del inicio de la infección por SARS-CoV-2, con una duración de al menos 2 meses sin ninguna causa que los explique. El CDC (Centro para el Control y Prevención de Enfermedades de Estados Unidos) lo define como un síndrome caracterizado por la persistencia de síntomas clínicos pasadas las 4 semanas del comienzo de la fase aguda de infección.2,3
Este síndrome representa una preocupación para la salud pública debido a la necesidad de los recursos médicos que exige y a la disminución de la productividad laboral.
Es un síndrome que puede afectar múltiples órganos (corazón, pulmón, riñón, hígado, cerebro, páncreas, el sistema inmunológico, el sistema digestivo, el sistema hematopoyético y el sistema osteoarticular). Por ende, los signos y síntomas incluyen un enorme abanico, desde autoinmunidad hasta trastornos de la coagulación, astenia, diabetes, deterioro cognitivo, trastornos en los ciclos menstruales, etc.1
Cualquiera que haya tenido infección por COVID puede presentar long COVID. Los factores de riesgo que se asocian a él son los siguientes: edad mayor de 65 años, sexo femenino, y el número y la gravedad de eventos agudos por COVID-19 padecidos.4
Se realizó un estudio prospectivo en la Unidad de Enfermedades Infecciosas de la Universidad de Campania con el objetivo de determinar la prevalencia de long COVID y sus características. Se incluyeron en total 427 pacientes entre marzo de 2020 y julio de 2022. El criterio de inclusión fue que hubieran sido pacientes hospitalizados por COVID. Al ingreso y en los meses 1, 3 y 6 posadmisión se recolectaron los siguientes datos: características clínicas, radiografía de tórax, y cuestionario que incluía astenia, disnea, tos, trastornos neuropsiquiátricos y artromialgias.
Al mes 6, solo 88 pacientes continuaban el seguimiento, lo cual implicó una limitación para el estudio (ver Cuadro 4).
De los pacientes, 83 presentaron long COVID versus 87 que no lo presentaron. En el primer grupo, el síntoma prevalente fue la disnea y, en segundo lugar, la astenia. A nivel radiológico, el vidrio esmerilado fue la imagen más frecuentemente encontrada en este grupo.

Conclusiones
• En esta cohorte se encontró una prevalencia de 19.4% de long COVID
• Disnea y astenia fueron los síntomas mayormente reportados durante las visitas de seguimiento entre los pacientes con long COVID.
• Al mes, los pacientes con long COVID reportaron una mayor incidencia de disnea y astenia.
• Se necesitan más estudios que recluten un mayor número de pacientes para determinar las características y prevalencia de este síndrome, y para evaluar posibilidades terapéuticas.
Referencias
1. Davis HE, et al. Long COVID: major findings, mechanisms and recommendations. Nat Rev Microbiol. 2023; 21:133–146.
2. Centers for Disease Control and Prevention. COVID-19. Long COVID or Post-COVID Conditions. Updated 2022 Dec 16. Disponible en https://www.cdc.gov/coronavirus/2019-ncov/long-term-effects/index.html#:~:text=People
3. World Health Organization. Post COVID-19 condition (Long COVID). 2022 Dec 7. Disponible en https://www.who.int/europe/news-room/fact-sheets/item/post-covid-19-condition#:~:text=It
4. O'Mahoney LL, et al. The prevalence and long-term health effects of Long Covid among hospitalised and non-hospitalised populations: a systematic review and meta-analysis. The Lancet. 2023;55:101762.
COVID-19 persistente en pediatría:aún queda mucho camino por recorrer
Dra. Lorenza Romani.
IRCCS-Bambino Gesú Children’s Hospital,
Roma, Italia
En general, los niños presentan un curso asintomático o leve de la infección por SARS-CoV-2. Los casos críticos son infrecuentes y se desarrollan en pacientes con comorbilidades graves. Las diferentes respuestas inmunes al virus de adultos y niños explican que el curso clínico en ambas poblaciones no sea comparable. Sin embargo, los niños pueden sufrir síntomas relacionados con COVID persistente (más allá de los 3 meses), en una prevalencia variable que va del 4% al 66%.1 No obstante, en pediatría, la información al respecto es muy heterogénea.
Un estudio unicéntrico italiano evaluó en forma prospectiva (2021-2022) el riesgo de desarrollar COVID persistente. Se incluyeron 273 pacientes, el 70% de los cuales cumplían criterios para ser clasificados como COVID persistentes. Los síntomas más frecuentes fueron fatiga (48.2%), tos (25.1%) y cefalea (20%).2
En la comparación de los grupos con COVID persistente y sin este, no se encontraron diferencias sustanciales, aunque se detectó que los pacientes con COVID persistente tenían más edad. Entre los grupos, no se hallaron diferencias en los resultados de electrocardiograma, espirometría o ecografía de pulmón (ver Cuadro 5).
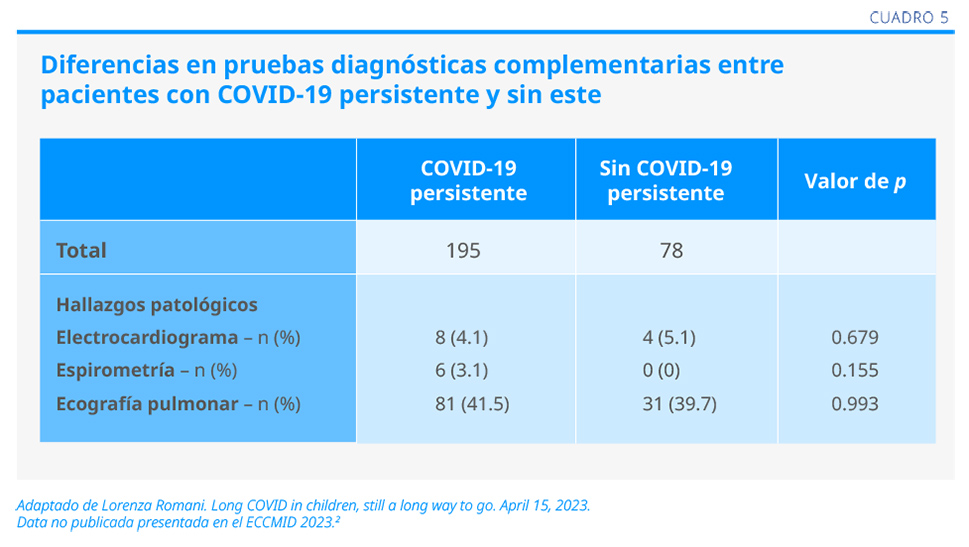
Conclusiones
• En los niños y adolescentes, son frecuentes los síntomas persistentes posinfección aguda por SARS-CoV-2.
• El estudio no reveló alteraciones pulmonares o cardíacas específicas en los pacientes con COVID-19 persistente.
• El análisis de los síntomas posCOVID debe realizarse con cuidado debido al solapamiento de situaciones sociales, como las consecuencias del aislamiento de la enfermedad.
• Se necesitan estudios de calidad para mejorar el entendimiento en el área.
Referencias
1. Fainardi V, et al. Long COVID in Children and Adolescents. Life (Basel). 2022 Feb 14;12(2):285.
2. Romani L, et al. Long COVID in children, still a long way to go. April 15, 2023. Data no publicada presentada en el ECCMID 2023.
Efectos del trasplante renal en el pronóstico y curso clínico del COVID-19:
Sohyun B, et al.
División de Enfermedades Infecciosas, Departamento de Medicina Interna, Escuela de Medicina,
Universidad Nacional de Kyungpook – Daegu, Corea
La mortalidad secundaria a la enfermedad por COVID-19 ha disminuido en la era ómicron1. Este estudio buscó determinar si los pacientes receptores de trasplante renal seguían siendo un grupo de riesgo con mayor mortalidad y progresión a cuadros graves del COVID-19 en la era ómicron en comparación con los pacientes sin trasplante renal.
Realizando un score de propensión, se incluyeron 128 pacientes con una media de edad de 57 años y en su mayoría hombres, en los cuales la mortalidad fue del 2.3%. Luego de ajustar por confundidores, se observó que el antecedente de trasplante renal se asociaba con un riesgo 6 veces mayor (OR 6.2; IC 95% 1.55-31.3; p=0.016) de requerir oxigenoterapia, además de observarse que el requerimiento de oxígeno se observaba más tardíamente de iniciados los síntomas (ver Cuadro 6).

Conclusiones
• Los pacientes receptores de trasplante renal tenían un mayor riesgo de progresar a formas graves de infecciones por COVID-19.
• En estos pacientes, la necesidad de oxigenoterpia se producía más tardíamente que en el grupo control.
Referencias
1. Ward IL, et al. Risk of covid-19 related deaths for SARS-CoV-2 omicron (B.1.1.529) compared with delta (B.1.617.2): retrospective cohort study. BMJ. 2022 Aug 2;378:e070695.
Complicaciones y evolución del COVID-19 en pacientes pediátricos con enfermedades hematoncológicas y en pacientes pediátricos trasplantados de médula ósea: un estudio retrospectivo en India
Krishna V, et al.
Apollo Hospitals. Chennai, India
Los pacientes con COVID-19 inmunocomprometidos tienden a tener un tiempo de carga viral más prolongado y una fase inflamatoria ausente o disfuncional. Se ha observado mayor mortalidad en pacientes con leucemia aguda, terapias complejas, trasplantados de médula ósea, síndromes mielodisplásicos de alto riesgo y terapias dirigidas al ag del receptor quimérico.1
El objetivo de este estudio fue evaluar el perfil clínico, las complicaciones y la evolución en pacientes con enfermedad hematoncológica (EHO) y en pacientes trasplantados de médula ósea (TMO) en una cohorte de pacientes pediátricos.
Se realizó un estudio retrospectivo observacional en un centro de tercer nivel en Chennai, India, en el cual se incluyeron pacientes menores de 18 años que presentaban EHO o TMO y que habían sido diagnosticados con COVID-19 entre enero de 2020 y septiembre de 2022. Se incluyeron 76 pacientes con una mediana de edad de 9 años, de los cuales 42% eran niños y 34% eran niñas
(ver Cuadro 7).2
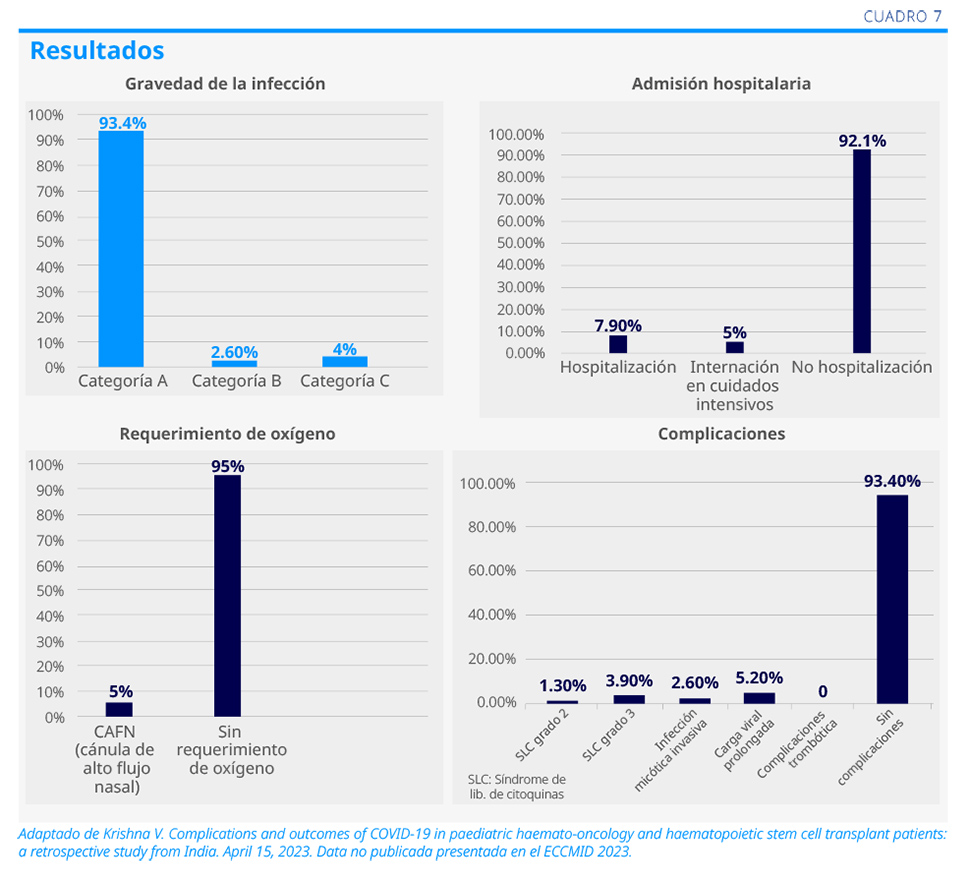
Conclusiones
• El COVID-19 produjo serias complicaciones en 42% de los pacientes pediátricos trasplantados de médula ósea, incluyendo una muerte.
• El síndrome de liberación de citoquinas fue la complicación más frecuente y, en segundo lugar, la infección micótica invasiva.
• En esta cohorte, los pacientes con enfermedad hematoncológica pediátrica presentaron COVID-19 leve.
Referencias
1. Haeusler GM, et al. SARS-CoV-2 in children with cancer or after haematopoietic stem cell transplant: An analysis of 131 patients. Eur J Cancer.
2021 Dec;159:78-86.
2. Krishna V, et al. Complications and outcomes of COVID-19 in paediatric haemato-oncology andhaematopoietic stem cell transplant patients: a
retrospective study from India. Poster Presentation EW0708, presented at ECCMID 2023.
Mortalidad por olas de SARS-CoV-2 en pacientes críticos y no críticos de un hospital terciario en la ciudad de México:
Dr. P. Castañeda-Méndez
Médica Sur Clinic Foundation. Ciudad de México, México
Este estudio prospectivo observacional tuvo como finalidad comparar la mortalidad y la tasa de vacunación en pacientes que fueron admitidos en el hospital con un diagnóstico de infección por SARS-CoV-2 durante las 5 olas que se presentaron en México.
Los resultados fueron los siguientes:1
• 1.a ola (alfa): 679 pacientes admitidos en el hospital con una mortalidad de 5.7%.
• 2.aa ola (beta): 886 pacientes con una mortalidad del 9.6%.
• 3.a ola (delta): 264 pacientes, 46% de pacientes vacunados. La mortalidad general es de 7.2%.
La mortalidad en pacientes vacunados es de 4.1% vs. 9.8% en no vacunados.
• 4.a ola (ómicron): 165 pacientes, 63.6% de pacientes vacunados. La mortalidad general es de 9.7%. La mortalidad en pacientes vacunados es de 4.8% vs. 18.3% en no vacunados.
• 5.a ola (variantes ómicron): continúa golpeando a México desde el 30 de mayo de 2022, con un total de 41 admisiones hasta julio. 73.2% de pacientes vacunados. La mortalidad general es de 2.4%. La mortalidad en pacientes vacunados es de 0% vs. 9.1% en no vacunados.
Conclusiones
• Los resultados de la pandemia por COVID-19 han cambiado debido a las campañas de inmunización que redujeron la mortalidad exitosamente en México.
• Durante las tres últimas olas, las vacunas ya estaban disponibles en este país; se observó una notable reducción de la mortalidad en comparación con las dos primeras olas.
Referencias
1. Castañeda Mendez, P. et al. Mortality per waves of SARS-CoV-2 in critical and non critical hospitalised COVID-19 patients in a tertiary care hospital in Mexico City. Abstrac E0358 presented at ECCMID 2023.
Factor de riesgo para infecciones nosocomiales en pacientes críticos con COVID-19; el uso temprano de antibióticos aumenta más el riesgo que la administración de corticoides
Preudtipong Noopetch, MD, MSc
Departamento de Medicina, Hospital Hatyai, Tailandia
Rutporn Benchamanon, MD
Departamento de Ginecología y Obstetricia, Hospital Hatyai, Tailandia
Los corticoides fueron un tratamiento de elección en la neumonía por el COVID-19. Al contribuir a un estado de inmunosupresión y aumentar el riesgo de infecciones,1 aumentó la prescripción médica de antibióticos en pacientes críticos con COVID-19.2 El objetivo del siguiente análisis fue evaluar el riesgo de infección nosocomial en pacientes críticos con COVID-19.
En este estudio de cohorte se evaluaron 257 pacientes críticos con COVID-19 confirmado, desde el 1 de abril de 2021 al 31 de marzo de 2022. Se obtuvo información directa de la atención de los pacientes y por medio de la historia clínica. El objetivo principal fue explorar qué factores de riesgo están asociados al aumento de infecciones nosocomiales en pacientes críticos con COVID-19, por medio del análisis multivariado por regresión logística.
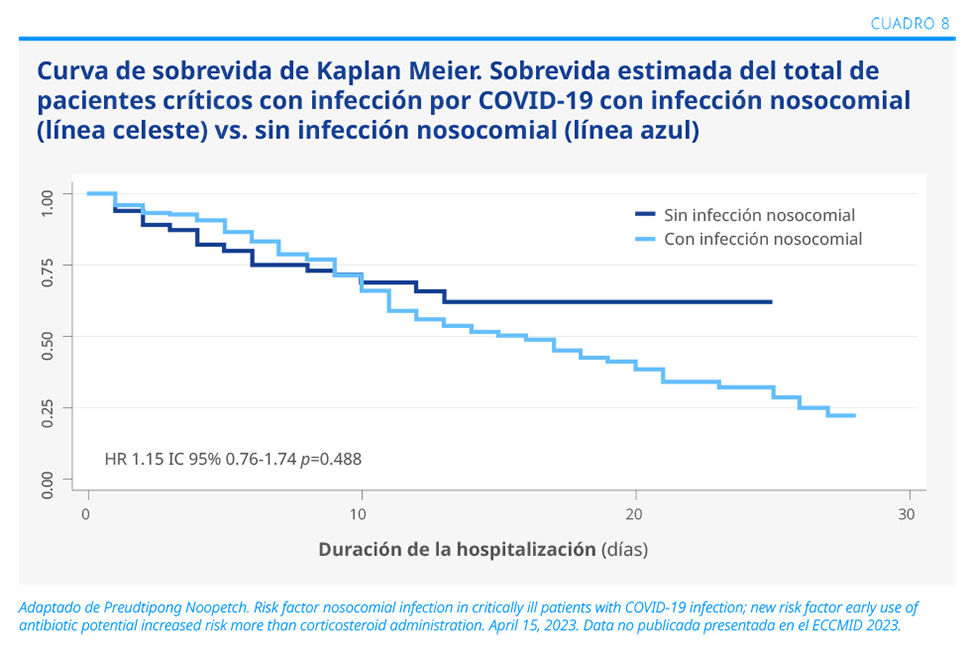
Se identificaron 120 pacientes con infecciones nosocomiales. Comparados con los pacientes sin infecciones nosocomiales, tuvieron una hospitalización más prolongada [13.76 (±0.81) vs. 7.78 (±0.38) días; p<0.001], más neumonía por COVID-19 [109 (90.83%) vs. 95 (69.34%); p<0.001], mayor requerimiento de ARM [99 (82.5%) vs. 42 (30.66%); p<0.001] y mayor administración temprana de antibióticos (indicados dentro de las primeras 24 h del ingreso) [100 (83.33%) vs. 63 (45.99%); p<0.001] (ver Cuadro 8).
La diabetes fue la comorbilidad preexistente más frecuente en los pacientes con infecciones nosocomiales y más casos que en los pacientes sin infecciones nosocomiales [87 (73.55%) vs. 63 (45.99%); p<0.001]. El análisis multivariado de odds ratios (OR) determinó que el mayor factor de riesgo para la infección nosocomial fue la ARM* (aOR 7.27; IC del 95% 3.03-17.45; p<0.001) seguido por hospitalización mayor a 10 días (aOR 3.67; IC del 95% 1.68-8; p=0.001) y el uso temprano de antibióticos (aOR 3.01; IC del 95% 1.39-6.5; p=0.005). El uso de corticoides no fue estadísticamente significativo (p=0.101, p=0.236 y p=0.137, respectivamente).
*ARM: Asistencia Respiratoria Mecánica
Conclusiones
• El requerimiento de ARM, la hospitalización prolongada, el uso temprano de antibióticos y la diabetes se asociaron con un mayor riesgo de infecciones nosocomiales en pacientes críticos con COVID-19.
• Probablemente por falta de poder estadístico en nuestro estudio, el uso de corticoides no estuvo asociado de manera significativa.
Referencias
1. Ahmed MH, et al. Dexamethasone for the Treatment of Coronavirus Diseases (COVID-19): a Review. SN Compr. Clin. Med. 2020;2:2637-2646.
2. Langford BJ, et al. Antibiotic prescribing in patients with COVID-19: rapid review and meta-analysis. Clin Microbiol Infect. 2021 Apr;27(4):520-531.
Identificación de recursos esenciales para responder a una pandemia: un estudio Delphi Internacional del proyecto EU-PANDEM-2
Beishuisen B, et al.
Centro para el Control de las Enfermedades Infecciosas,
Instituto Nacional de Salud Pública y Ambiente.
Bilthoven, Países Bajos.
El estudio tuvo como objetivo identificar (por medio de un consenso Delphi) los recursos esenciales en la salud pública y la atención clínica para la planificación de una pandemia, en el contexto de una enfermedad respiratoria viral emergente. Un panel de expertos en salud pública y un panel de médicos participaron en el cuestionario y en una ronda de consenso en línea.
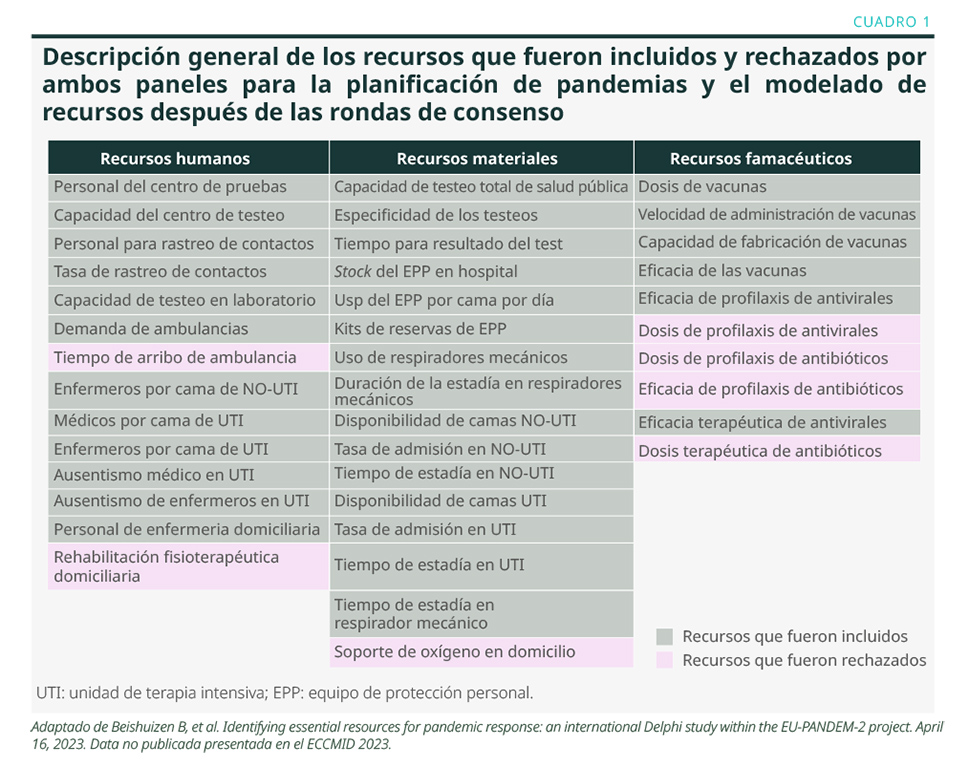
Se observó consenso entre los dos paneles sobre 40 recursos (33 incluidos y siete rechazados) (ver Cuadro 1).1 No se observó consenso en 13 recursos. Surgieron doce recursos adicionales y se incluyeron once, como equipos de protección personal para equipos móviles, recursos para atención primaria y recursos relacionados con la ventilación mecánica.
Conclusiones
• Este estudio destaca un conjunto de recursos esenciales para priorizar al momento de realizar actividades de preparación para una pandemia, y también destaca la importancia de incluir expertos en salud pública como médicos de clínicos.
• La inclusión de estos recursos en modelos y escenarios pandémicos para ejercicios de preparación permitirá abordar las brechas de recursos y permitir una toma de decisiones basada en la evidencia durante futuros brotes, epidemias o pandemias.
Referencias
1. Beishuizen B, et al. Identifying essential resources for pandemic response: an international Delphi study within the EU-PANDEM-2 project. April16,
2023. Data no publicada presentada en el ECCMID 2023.
Cambio en la carga viral del SARS-CoV-2 observado con tres terapias diferentes para COVID-19: el estudio MONET
Dra. Valentina Mazzotta
Instituto Nacional de Enfermedades Infecciosas Lazzaro Spallanzani
Roma, Italia.
En enero de 2022, durante la ola de ómicron, se encontraban disponibles anticuerpos monoclonales (mAbs, por sus siglas en inglés) como moléculas antirretrovirales, para el tratamiento en la fase temprana de la enfermedad de pacientes con COVID-19 de leve a moderado y con alto riesgo de progresión.
En estudios in vitro, se observó una caída de la capacidad neutralizante viral de los mAbs frente a la variante ómicron. Esto sugiere la posibilidad de falta de eficacia de los mAbs ante esta cepa.1
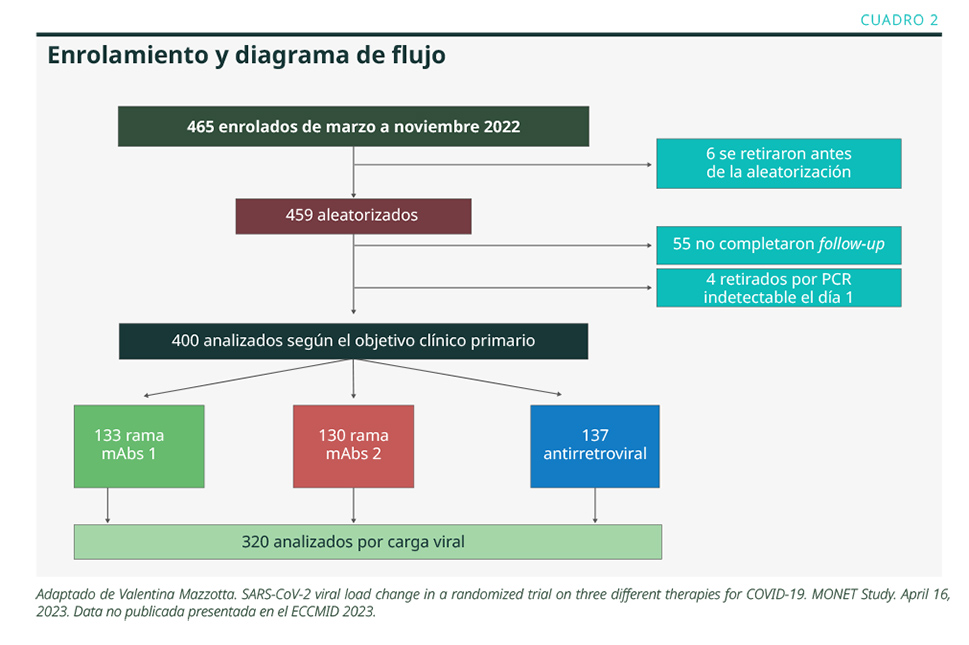
MONET es un estudio de fase IV, abierto, multicéntrico y aleatorizado. Su objetivo es evaluar la eficacia clínica y virológica de diferentes tratamientos tempranos contra el COVID-19 leve y moderado en pacientes ambulatorios de alto riesgo. Los pacientes debían ser enrolados en los primeros 5 días de infección y tener una prueba de laboratorio viral positiva por antígeno o PCR. El estudio fue llevado a cabo por la agencia italiana de fármacos (AIFA). Los criterios de exclusión destacables fueron insuficiencia renal o hepática severa, antecedente de infarto de miocardio, interacciones medicamentosas inmanejables, riesgo alto de sangrado y VIH activo no tratado. Los pacientes fueron aleatorizados a 3 ramas en una relación 1:1:1. Dos de las ramas recibían tratamiento con mAbs y, la tercera, con la asociación de 2 antirretrovirales (1 inhibidor peptidomimético de la proteasa principal del SARS-CoV-2 más un antirretroviral inhibidor de proteasa). En total, se aleatorizaron 459 pacientes, de los cuales 400 completaron el seguimiento para la evaluación de la eficacia clínica. En 320 de ellos, pudo evaluarse la carga viral (ver Cuadro 2). El seguimiento clínico fue de 29 días. Los endpoints primarios fueron muerte u hospitalización por cualquier causa y/o progresión a COVID-19 severo. El objetivo secundario fue determinar la presencia o no de virus en hisopado nasal por PCR en los días 7 y 29.2
Observaciones principales
• No se observaron muertes en ninguna rama.
• Se produjeron 5 hospitalizaciones, todas en las ramas que recibían mAbs.
• La caída de la carga viral en el día 7 fue significativamente mayor en el grupo que recibía antirretrovirales que en los grupos que recibían mAbs.
Conclusiones
• El riesgo total acumulado de falla clínica en COVID-19 leve en la era de ómicron es bajo.
• El análisis de la progresión clínica en las tres ramas sugiere que los pacientes que reciben antirretrovirales podrían presentar mejor evolución, comparados con aquellos que reciben mAbs. Sin embargo, los resultados no son concluyentes debido al número bajo de participantes del estudio.
• Este estudio provee evidencia clínica de la ventaja que el uso de antirretrovirales tendría frente a los mAbs cuando se utilizan en pacientes con la cepa ómicron.
• Los resultados del estudio coinciden con lo observado in vitro, lo que sugiere que los mAbs no mantendrían su capacidad neutralizante viral frente a la cepa ómicron.
Referencias
1. Takashita E, et al. Efficacy of Antibodies and Antiviral Drugs against Omicron BA.2.12.1, BA.4, and BA.5 Subvariants. N Engl J Med 2022;387(5):468-470.
2. Mazzotta, V. SARS-CoV-2 viral load change in a randomized trial on three different therapies for COVID-19. MONET Study. April 16, 2023.Data no publicada presentada en el ECCMID 2023.
Diferencias en la presentación clínica y resultados de las infecciones respiratorias virales en las edades extremas
Siran Keske, MD
Profesor Asociado del Departamento de Enfermedades Infecciosas y Microbiología Clínica. Hospital Americano Estambul, Turquía
La población de adultos mayores se está incrementando en el mundo. Existen características especiales en esta población que la hacen más susceptible a las infecciones virales (ver Cuadro 3).1
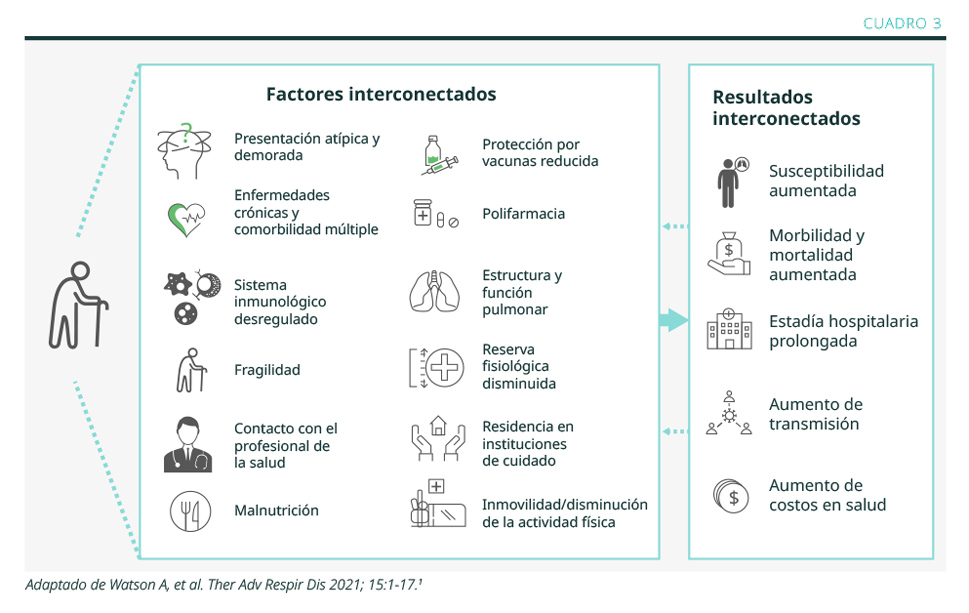
La presentación clínica suele ser diferente a esta edad: pueden no presentar fiebre, el examen físico puede ser normal, también el recuento de glóbulos blancos (incluso con infecciones bacterianas agregadas), la Rx de tórax puede ser normal en los primeros días, el deterioro cognitivo previo puede afectar el reconocimiento de los signos y síntomas y retrasar el diagnóstico, la neumonía aspirativa es una complicación común en pacientes con deterioro neurológico,2 pueden presentar disminución del apetito, presentarse solo con insuficiencia renal por disminución de la ingesta de líquidos, o con hiperglucemia, sin otros síntomas. A pesar de que la infección por el virus sincicial respiratorio (VSR) representa un síndrome clínico diferente al de la infección por influenza A en los adultos mayores, caracterizado por congestión nasal y sibilancias, no es factible distinguir entre ambos virus solamente por la clínica. La protección inmunológica después de la infección por el VSR disminuye con la edad, lo que puede ser un factor de riesgo para presentar reinfecciones por el VSR.3
La mortalidad por infecciones virales es mayor en sujetos de más de 75 años, siendo el VSR y la influenza A los virus asociados más frecuentes.4 La mortalidad en sujetos con coinfección bacteriana y viral es mayor que con la infección aislada viral o bacteriana.5 Algunos patógenos, como los rinovirus, que causan cuadros leves en la población general, pueden ser fatales en los adultos mayores.6
Conclusiones
Los adultos mayores
• Suelen tener presentaciones clínicas atípicas, que demoran el diagnóstico y el tratamiento.
• Presentan menor protección frente a las infecciones virales.
• Suelen tener infecciones concomitantes (neumonía, infección urinaria, sepsis) que empeoran el pronóstico.
• Presentan mayores tasas de internación en cuidados intensivos y de mortalidad.
• Los virus sincicial respiratorio y parainfluenza presentan las mayores dificultades para el manejo médico.
Recomendaciones
• La formación de profesionales en infecciones geriátricas.
• La vacunación a los pacientes (influenza, neumococo).
• El diagnóstico precoz (por antígenos y/o PCR).
• El tratamiento antiviral precoz.
• Un seguimiento estrecho para detectar infecciones secundarias. La nutrición adecuada y la prevención de neumonía aspirativa.
• Las vacunas y los tratamientos antivirales efectivos para VSR.
Referencias
1. Watson A, et al. Respiratory viral infections in the elderly. Ther Adv Respir Dis 2021; 15:1753466621995050. doi: 10.1177/1753466621995050.
2. Keske S, Differences in the clinical presentation and outcomes of respiratory viral infections at the extremes of age. April 16, 2023. Data no publicada presentada en el ECCMID 2023.
3. Terrosi C, et al. Short Report: Humoral Immunity to Respiratory Syncytial Virus in Young and Elderly Adults. Epidemiol Infect 2009; 137: 1684-86.
4. Van Asten L, et al. Mortality attributable to 9 common infections: significant effect of influenza A, respiratory syncytial virus, influenza B, norovirus,and parainfluenza in elderly persons. J Infect Dis 2012; 206(5): 628-39. doi: 10.1093/infdis/jis415.
5. Liu Y, et al. Outcomes of respiratory viral-bacterial co-infection in adult hospitalized patients. EClinicalMedicine. 2021; 37:100955.doi: 10.1016/j.eclinm.2021.100955.
6. Louie J, et al.. Rhinovirus Outbreak in a Long Term Care Facility for Elderly Persons Associated with Unusually High Mortality. Clinical Infectious Diseases 2005; 41(2): 262-265.
El impacto del diagnóstico en la temporalidad del tratamiento antiviral de la influenza, el Virus Sincicial Respiratorio y el COVID-19
Giulia De Angelis
Universidad Católica del Sagrado Corazón, Hospital Universitario A. Gemelli
Roma, Italia
En pacientes con síntomas o sospecha de infecciones respiratorias, actualmente se utilizan técnicas de detección viral basadas en biología molecular, con el fin de obtener resultados en menos tiempo.1 Los laboratorios de microbiología tuvieron que adaptarse durante la pandemia por COVID-19 para responder al incremento de estudios diagnósticos, no solo de SARS-CoV-2, sino también de otros virus respiratorios, tratando de obtener estos resultados en el menor tiempo posible.2 Esto fue posible a través del uso de pruebas de reacción en cadena de la polimerasa (PCR) múltiples, cuya principal característica es detectar varios virus en cortos periodos de tiempo.3
Durante la primera parte de la pandemia, debido a las medidas adoptadas para reducir el contagio de SARS-CoV-2, se observó una reducción en la circulación de otros virus respiratorios, mientras que, en la parte final de la pandemia, se observó un incremento en la circulación de estos virus, los cuales coexistían temporalmente.4 Si los tiempos de resultado son menores, también se deduce que se reduciría el tiempo de inicio de los tratamientos antivirales y el uso de tratamientos innecesarios. En este sentido, el estudio FluPOC evaluó en 613 pacientes la proporción con confirmación de influenza que recibieron tratamiento antiviral en los primeros 5 días de internación.5 Excluyendo a los pacientes que recibieron tratamiento en forma empírica, el grupo en el que se obtuvo el resultado con un test rápido point-of-care recibió tratamiento más rápido y en una mayor proporción de pacientes en comparación con el grupo control (ver Cuadro 4). La evidencia en infecciones por virus sincisial respiratorio es menor (posiblemente debido a que el tratamiento antiviral en estos cuadros en controversial). Por otro lado, cuando se evalúa el uso de estas pruebas y la asociación con la prescripción de tratamientos antibióticos, los resultados también son controversiales.
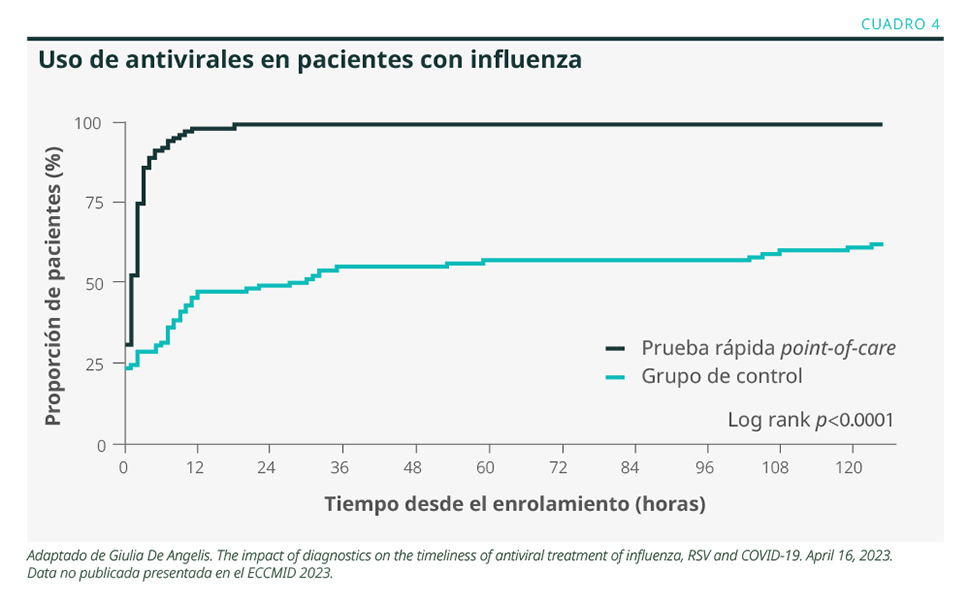
Conclusiones
• La pandemia por COVID-19 colaboró con la clarificación de la patogénesis viral, permitiendo un avance diagnóstico.
• El uso de pruebas diagnósticas reduce los tiempos de inicio de los tratamientos antivirales.
• El uso de estas pruebas podría limitar el uso de tratamientos inadecuados para infecciones virales, con todo el impacto negativo que esto conlleva.
Referencias
1. Uyeki TM, et al. Influenza. Lancet. 2022 Aug 27;400(10353):693-706. doi: 10.1016/S0140-6736(22)00982-5. PMID: 36030813; PMCID:PMC9411419.
2. Posteraro B, et al. FPG COVID Laboratory Group. Clinical microbiology laboratory adaptation to COVID-19 emergency: experience at a large teaching hospital in Rome, Italy. Clin Microbiol Infect. 2020 Aug;26(8):1109-1111. doi: 10.1016/j.cmi.2020.04.016. Epub 2020 Apr 21.PMID:32330569; PMCID: PMC7172783.
3. Huang HS, et al. Multiplex PCR system for the rapid diagnosis of respiratory virus infection: systematic review and meta-analysis. Clin Microbiol Infect. 2018 Oct;24(10):1055-1063.
4. Chow EJ, et al. The effects of the COVID-19 pandemic on community respiratory virus activity. Nat Rev Microbiol. 2023 Mar;21(3):195-210. doi:10.1038/s41579-022-00807-9. Epub 2022 Oct 17. PMID: 36253478; PMCID: PMC9574826.
5. Clark TW, et al. Clinical impact of a routine, molecular, point-of-care, test-and-treat strategy for influenza in adults admitted to hospital (FluPOC): a multicentre, open-label, randomised controlled trial. Lancet Respir Med. 2021 Apr;9(4):419-429. doi: 10.1016/S2213-2600(20)30469-0. Epub 2020 Dec 4. PMID: 33285143; PMCID: PMC9764870.
De los ensayos clínicos a la práctica clínica: evolución del manejo del COVID-19, el Virus Sincicial Respiratorio y la influenza en Estados Unidos
Dr. Michael G. Ison
Jefe de Enfermedades Respiratorias, DMID/NIAID/NIH
Estados Unidos
Los principales grupos de riesgo para desarrollar enfermedad severa por influenza son los niños menores de 5 años, las personas mayores de 65 años o con comorbilidades, y las embarazadas.1 Para los pacientes con influenza atendidos de forma ambulatoria, las guías proponen iniciar antivirales en los adultos y niños con riesgo de desarrollar complicaciones, independientemente de que hubieran recibido vacunación.2 Sugieren utilizar un inhibidor de la neuraminidasa o un inhibidor de endonucleasa de ARN.2 Las recomendaciones son similares para los pacientes que requieren internación con diagnóstico o sospecha de infección por influenza. Además, no se recomienda la indicación de rutina de corticoides o inmunomoduladores.2
En la infección por influenza, es muy importante el inicio temprano de la terapia antiviral, cuando está indicada. En un estudio retrospectivo de 699 pacientes, el inicio en las primeras 6 horas desde la admisión redujo la duración de la internación y la mortalidad (0 versus 4.5%).3
El Virus Sincicial Respiratorio (VSR) afecta especialmente a los pacientes inmunocomprometidos. La terapia antiviral demostró beneficio en los modelos de desafío farmacológico (Pharmacological Challenge Models), aunque los resultados clínicos no son tan claros.4
En el COVID-19, se plantean diferentes desafíos respecto a la terapia antiviral, considerando que la vacunación redujo drásticamente la mortalidad.5 Cuáles pacientes inmunocompetentes se benefician con la terapia antiviral y el rol de los biomarcadores en el inicio del tratamiento son algunos ejemplos de las cuestiones que, por el momento, no tienen una respuesta inobjetable.5
En la actualidad, la implementación de la terapia viral es un verdadero desafío debido a las barreras de acceso. En el Cuadro 5, se muestran datos de la implementación de la terapia antiviral en la infección por influenza.6
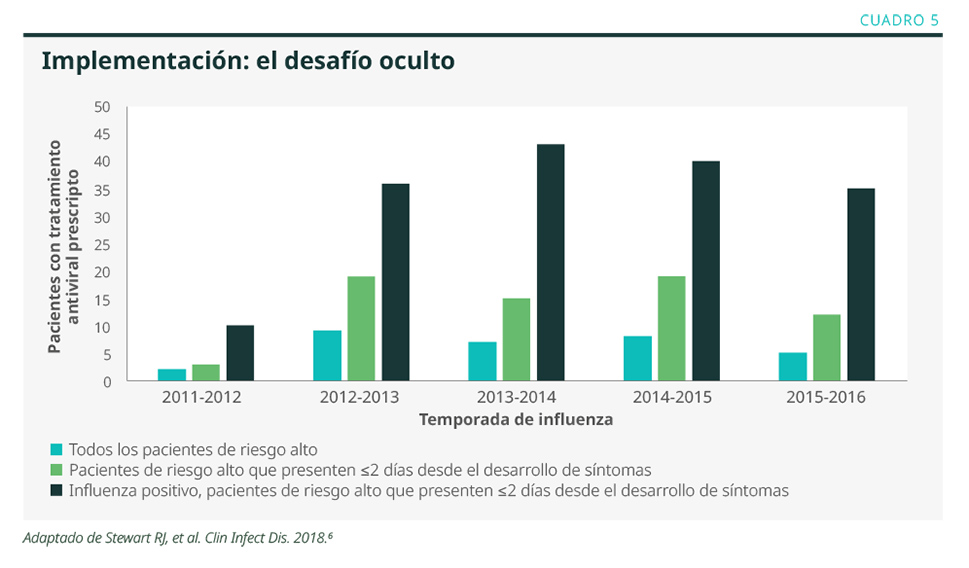
Conclusiones
• En los últimos años, se lograron importantes avances en la terapia antiviral. Sin embargo, el acceso y la implementación son desafíos que aún requieren esfuerzo para optimizarse.
Referencias
1. Writing Committee of the WHO Consultation on Clinical Aspects of Pandemic (H1N1) 2009 Influenza. Clinical aspects of pandemic 2009 influenza A (H1N1) virus infection. N Engl J Med. 2010 May 6;362(18):1708-19.
2. Uyeki TM, et al. Clinical Practice Guidelines by the Infectious Diseases Society of America: 2018 Update on Diagnosis, Treatment, Chemoprophylaxis, and Institutional Outbreak Management of Seasonal Influenza. Clin Infect Dis. 2019 Mar 5;68(6):e1-e47.
3. Katzen J, et al. Early Oseltamivir After Hospital Admission Is Associated With Shortened Hospitalization: A 5-Year Analysis of Oseltamivir Timing and Clinical Outcomes. Clin Infect Dis. 2019 Jun 18;69(1):52-58.
4. Marty FM, et al. A Phase 2b, Randomized, Double-blind, Placebo-Controlled Multicenter Study Evaluating Antiviral Effects, Pharmacokinetics, Safety, and Tolerability of Presatovir in Hematopoietic Cell Transplant Recipients with Respiratory Syncytial Virus Infection of the Lower Respiratory Tract. Clin Infect Dis. 2020 Dec 31;71(11):2787-2795.
5. Ison MG. From Clinical Trials to Clinical Practice: Evolution of the management of COVID, RSV and Influenza in North America. April 16, 2023. Data no publicada presentada en el ECCMID 2023.
6. Stewart RJ, et al. Influenza Antiviral Prescribing for Outpatients With an Acute Respiratory Illness and at High Risk for Influenza-Associated
Complications During 5 Influenza Seasons-United States, 2011-2016. Clin Infect Dis. 2018 Mar 19;66(7):1035-1041.
CORONACHEK: un sistema de autoevaluación y triaje para el COVID-19 en Suiza
Dr. Ludovico G. Cobuccio
Hospital Universitario de Lausanne
Suiza.
Con el fin de responder al incremento de la demanda de testeos, reducir la carga laboral en los profesionales de la salud y obtener información confiable, el Dr. Cobuccio diseñó un prototipo a partir de un chatbot con la aplicación Telegram, que se basaba en la pesquisa de síntomas a pacientes que cumplían con criterios diagnósticos. Luego, a estos pacientes se les ofrecía un test rápido a domicilio y la posibilidad de realizar una teleconsulta. El primer paso fue analizar las recomendaciones tanto locales como de la Organización Mundial de la Salud. En segundo lugar, se diseñó un algoritmo de decisiones que el equipo de informática adaptó a un lenguaje de lógica de lectura de máquinas (machine learning). Por último, se diseñó la interfase para el usuario, que resultó una aplicación para dispositivos móviles utilizada por más de 2.7 millones de personas, incluyendo otros países además de Suiza (ver Cuadro 1).
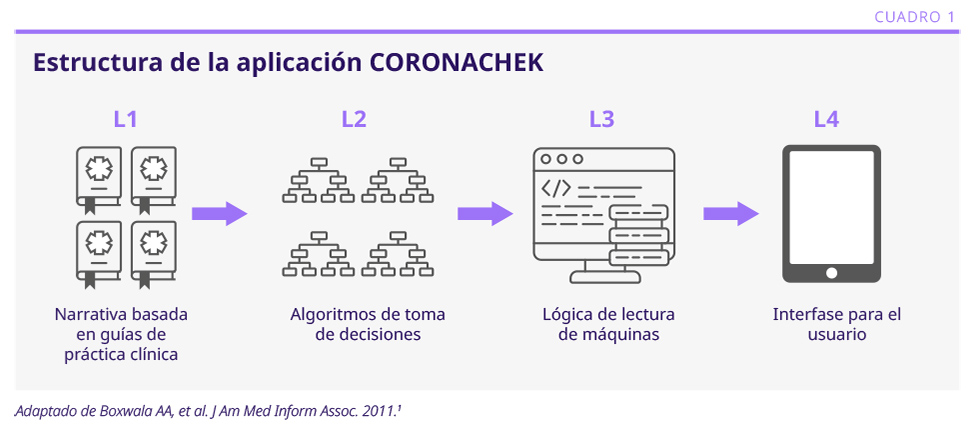
Conclusiones
• CORONACHEK satisfizo necesidades simples, pero importantes, durante la pandemia por el COVID-19.
• CORONACHEK colaboró con la coordinación y gestión de la afluencia de pacientes durante este período.
Referencias
1. Boxwala AA, et al. A multi-layered framework for disseminating knowledge for computer-based decision support. J Am Med Inform Assoc 2011;18:i132-i139.
Prevalencia e historia natural de la fatiga post infección en adultos y niños
Dr. Ben Katz
Profesor de pediatría, Escuela de Medicina de la Universidad Northwestern
Médico Asistente de la División de Enfermedades Infecciosas
Hospital de Niños Ann & Lurie
Chicago, Estados Unidos.
La fatiga crónica es un motivo de consulta muy frecuente. Alrededor de la mitad de los pacientes que completan los criterios para el síndrome de fatiga crónica (SFC) identifican el comienzo de su enfermedad a partir de una infección: fatiga post infecciosa (FPI).
El SFC asociado a mononucleosis infecciosa se ha utilizado como modelo de estudio para la FPI. El diagnóstico del SFC es sindromático. Existen varias definiciones, de las cuales tres se utilizaron en los trabajos que se representarán: la definición de Fukuda del Instituto Nacional de Salud (NIH 1994),1 el Consenso de Criterios de Canadá (2003)2 y los Criterios del Instituto de Medicina (IOM 2015)3. Los criterios más específicos son la fatiga inexplicable de más de 6 meses de duración, el deterioro en la concentración/memoria a corto plazo, malestar post ejercicio de más de 24 horas de duración y sueño no reparador. Es importante precisar la gravedad y frecuencia de los síntomas para realizar el diagnóstico.4 Se definieron como casos de SFC grave aquellos pacientes que alcanzaban más de 1 conjunto de criterios (por ej., Fukuda y Canadá, o Fukuda e IOM)
En un primer estudio de incidencia se realizó el seguimiento durante dos años de cerca de 300 adolescentes con diagnóstico de mononucleosis infecciosa.5 El 13% de ellos alcanzaron criterios de SFC a los 6 meses, el 7% persistieron a los 12 meses y el 4% a los 24 meses, con predominio en mujeres.
Un segundo estudio prospectivo realizó el seguimiento de 4500 escolares sanos, de los cuales el 5% presentaron mononucleosis infecciosa, y fueron reevaluados a los 6 meses para presencia de SFC. El seguimiento previo y posterior fue mediante cuestionarios de salud, fatiga, alteraciones autonómicas, ansiedad, depresión, estrés y síntomas autonómicos. Se tomaron muestras de sangre en cada etapa. El 23% de los niños cumplieron los criterios de SFC a los 6 meses, 8% de SFC grave, con predominio en mujeres.6 Presentaron diferencias significativas en todos los cuestionarios, con puntajes de mayor gravedad, los que presentaron SFC grave vs. SFC vs. controles (ver Cuadro 2).6 Los estudiantes que presentaron cuadros graves de mononucleosis tuvieron 3.3 veces más riesgo de presentar SFC grave (p<0.05).6 Se encontraron diferencias en los niveles de interleuquinas, principalmente en IL-13, desde el inicio en aquellos que posteriormente desarrollaron SFC.6 Se estudiaron 256 metabolitos en las diferentes etapas; se encontraron diferencias en 8 de ellos, entre aquellos que se recuperaron de la mononucleosis y en los que presentaron SFC. Estos metabolitos pertenecen a las vías del metabolismo del glutatión, nucleótidos, el ciclo de ácidos tricarboxílicos, la glucólisis y el ciclo de la urea, vías esenciales para la proliferación celular.
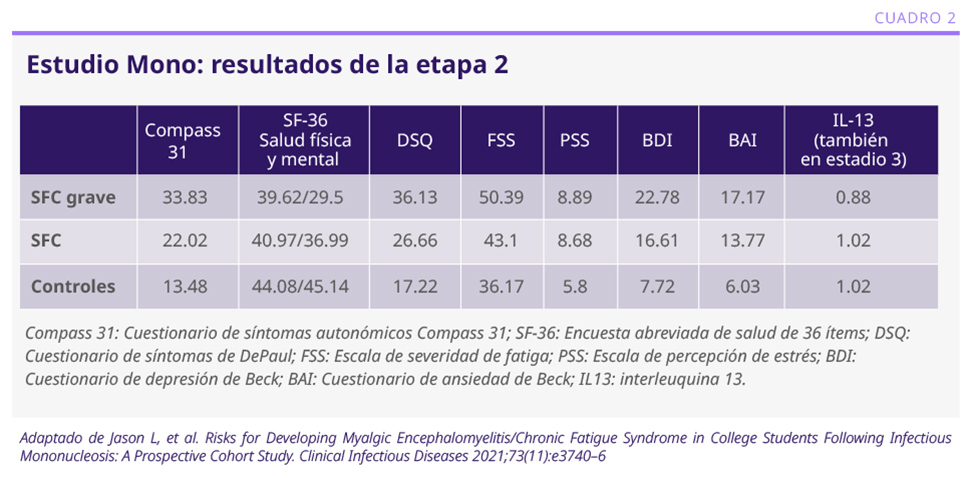
Conclusiones
• La mayoría de los pacientes tiende a recuperarse de la mononucleosis infecciosa.
• El grupo que desarrolló SFC grave tenía más fatiga y diferencias metabolómicas y en las citoquinas, al menos 6 semanas antes de enfermarse.
• Los cuadros más severos de mononucleosis infecciosa tendieron a presentar SFC grave.
Referencias
1. Fukuda K, et al. The chronic fatigue syndrome: a comprehensive approach to its definition and study. International Chronic Fatigue Syndrome Study Group. Ann Intern Med 1994; 121(12):953-9.
2. Carruthers B, et al. Myalgic Encephalomyelitis/Chronic Fatigue Syndrome: Clinical Working Case Definition, diagnostic and treatment protocols. Journal of Chronic Fatigue Syndrome 2003;11(1): 7-115.
3. Centers for Disease Control and Prevention. IOM 2015 Diagnostic Criteria [Internet]. Centers for Disease Control and Prevention. Citada el 17 de abril de 2023. Disponible en https://www.cdc.gov/me-cfs/healthcare-providers/diagnosis/iom-2015-diagnostic-criteria.html.
4. Jason L, et al. Examining case definition criteria for chronic fatigue syndrome and myalgic encephalomyelitis. Fatigue 2014; 2(1): 40-56.
5. Katz B, et al. Chronic fatigue syndrome after infectious mononucleosis in adolescents. Pediatrics 2009; 124(1):189-193.
6. Jason L, et al. Risks for Developing Myalgic Encephalomyelitis/Chronic Fatigue Syndrome in College Students Following Infectious Mononucleosis: A Prospective Cohort Study. Clin Infect Dis 2021;73(11):e3740-e3746.
La prevalencia y la historia natural del COVID prolongado en adultos y niños
Profesor Piush Mandhane MD, PhD, FRCPC
Stollery Children´s Hospital y Universidad de Alberta
Canadá
Definición
La OMS define al COVID subagudo/crónico como la persistencia de síntomas más allá de los 3 meses de la infección por SARS-CoV-2, con una duración de al menos dos meses, sin una explicación alternativa.1
Síntomas
La fatiga es uno de los más prominentes y el más frecuente, tanto en pacientes hospitalizados como en los no hospitalizados. También son frecuentes las alteraciones del sueño, la disnea, las palpitaciones y los cambios cognitivos.
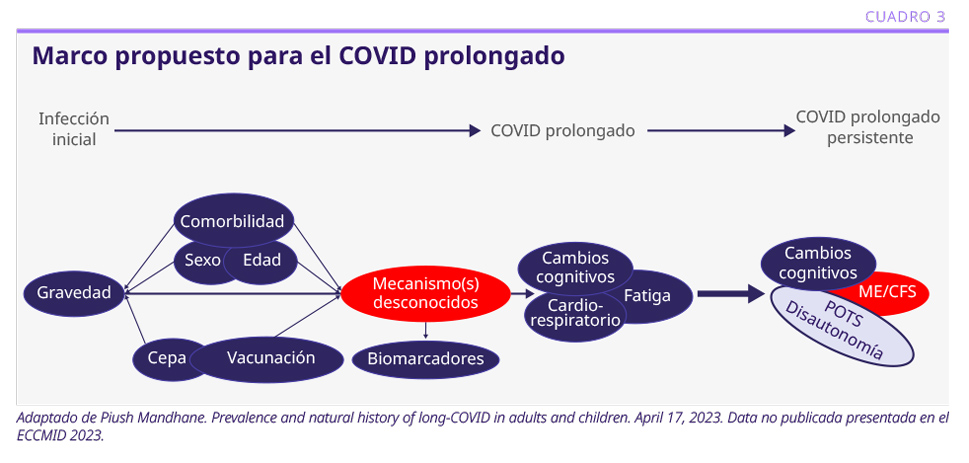
Los síntomas del COVID prolongado tienden a agruparse en tres fenotipos:
• Predominio de síntomas cardiorrespiratorios (adultos menores de 60 años, con comorbilidades físicas y enfermedad aguda grave).
• Predominio de fatiga como síntoma principal (asociado a dolor corporal o cambios del estado de ánimo, depresión y ansiedad). Esto en general se observa en mujeres con internaciones prolongadas.
• Predominio de síntomas cognitivos (niebla cerebral). Más frecuente en quienes tienen comorbilidades físicas, antecedentes de enfermedades mentales, enfermedad aguda grave o internaciones prolongadas.2
Factores de riesgo para el COVID prolongado
Un tercio de los pacientes con COVID prolongado no presenta factores de riesgo para esta afección.
El COVID prolongado parece estar vinculado a la gravedad de la infección inicial. El sexo femenino y la edad mayor a 40 años parecieran incrementar el riesgo de sufrir COVID prolongado.3 Es posible que el riesgo de COVID prolongado varíe de acuerdo con la cepa que causa la infección inicial, pero la disminución de riesgo que se observa en infecciones por la cepa ómicron (en comparación con las cepas beta y delta) puede ser producto del efecto confundidor de las inmunizaciones previas.
Duración de los síntomas del COVID prolongado
La fatiga, los problemas de concentración y memoria, la anosmia y la ageusia pueden persistir dos años después de la infección inicial. Los pacientes con COVID prolongado pueden presentar encefalomielitis miálgica/síndrome de fatiga crónica (EM/CFS), así como síndrome de taquicardia postural ortostática (POTS).4
Niños y COVID prolongado
En el caso de los niños, la identificación de casos de COVID prolongado se dificulta por el hecho de que existe un sesgo que disminuye el diagnóstico de infección por COVID en esta población. Como en los adultos, la gravedad de la infección inicial puede influenciar la duración de síntomas.
Los mecanismos que generan el COVID prolongado son desconocidos, aunque se hipotetiza que, en los casos menos graves, podría estar vinculado a la activación de respuestas fisiológicas adversas y, en los casos más severos, a la existencia de daño tisular y cicatrización de estas lesiones.5 El abordaje terapéutico del COVID prolongado aún es desconocido (ver Cuadro 3).
Conclusiones
• El COVID prolongado (la persistencia de síntomas a más de 3 meses de la infección inicial) está relacionado con la gravedad de la infección inicial. La fatiga, los cambios cognitivos, la anosmia, la disgeusia y las manifestaciones disautonómicas, como el síndrome de taquicardia postural ortostática, pueden persistir muchos meses.
• Es menos frecuente en la infección con el linaje ómicron, pero esto puede deberse también al efecto protector de la vacunación previa.
Referencias
1. World Health Organization. Post COVID-19 condition (Long COVID) [Internet]. 2022 Dec 7. World Health Organization. Citada el 17 de abril de 2023. Disponible en https://www.who.int/europe/news-room/fact-sheets/item/post-covid-19-condition#:~:text=It
2. Davis HE, et al. Long COVID: major findings, mechanisms and recommendations. Nat Rev Microbiol. 2023;21, 133–146. https://doi.org/10.1038/s41579-022-00846-2.
3. Tsampasian V, et al. Risk Factors Associated With Post-COVID-19 Condition: A Systematic Review and Meta-analysis. JAMA Intern Med. 2023 Mar 23:e230750.
4. Wahlgren C, et al. Two-year follow-up of patients with post-COVID-19 condition in Sweden: a prospective cohort study. Lancet Reg Health Eur. 2023 Feb 24:100595
5. Iwasaki A, et al. Why we need a deeper understanding of the pathophysiology of long COVID. Lancet Infect Dis. 2023 Apr;23(4):393-395. doi: 10.1016/S1473- 099(23)00053-1. Epub 2023 Feb 14. PMID: 36967698; PMCID: PMC9928485.
Resultados fisiológicos y reportados por pacientes más de 2 años después del COVID-19
Knut Stavem, MD, MPH, Ph. D.
Departmento de Medicina Pulmonar, Hospital Universitario Akershus
Lørenskog, Noruega
Se presentan los resultados preliminares de un estudio de seguimiento de una cohorte con COVID-19 (confirmada por PCR) durante 30 meses, cuyo objetivo fue determinar la prevalencia de fatiga y disnea, la asociación con la gravedad de la enfermedad aguda, la asociación con resultados objetivables y la comparación con la población general.
Se evaluaron pacientes de 18 años o más, no hospitalizados, pertenecientes al área de dos hospitales de Noruega, que se contactaron a través de tres laboratorios, en donde se realizaron las pruebas para COVID-191. Se seleccionaron 1000 pacientes, a quienes se les realizaron cuestionarios a los 3, 8, 14 y 30 meses. El cuestionario incluyó síntomas de COVID-19, disnea, calidad de vida, distrés psicológico y fatiga. Después de 6 meses, se agregaron cuestionarios de salud mental, pruebas funcionales respiratorias, pruebas cognitivas, pruebas de ejercicio y análisis de laboratorio. El número de respondedores a los 3, 8, 14 y 30 meses fue de 458, 310, 268 y 220, respectivamente. Los síntomas más frecuentes a los 3 meses fueron: disnea y alteraciones del gusto o el olfato.2 A los 8 meses fueron: disnea (36%, en la mayoría de los casos, leve), mialgia (26%), artralgia (26%), pérdida del olfato (20%), debilidad muscular (30%) y alteraciones del sueño (32%). La proporción de fatiga con el uso del cuestionario FSQ11 se mantuvo entre 40-50% a lo largo del estudio (ver Cuadro 4).
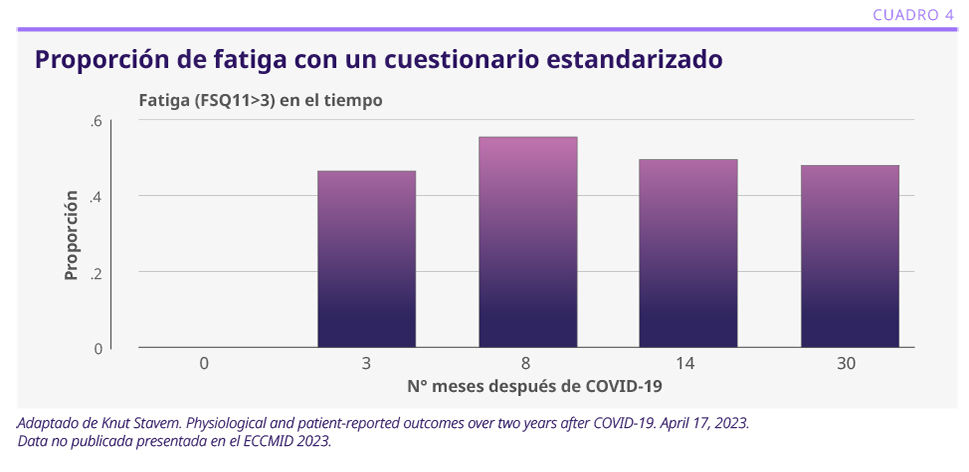
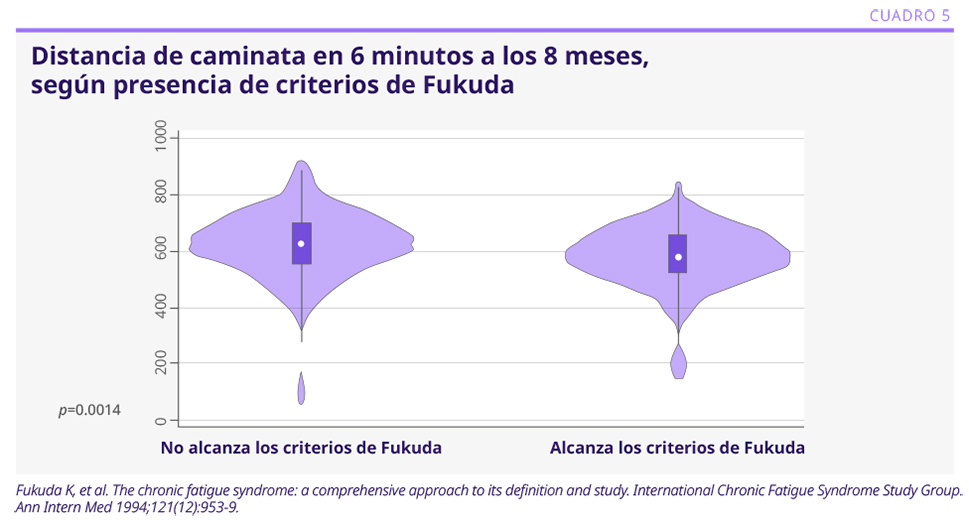
Con otros criterios, como los de Fukuda,3 la prevalencia fue menor, de alrededor del 20%. Los cuestionarios de calidad de vida a los 3 meses no mostraron mayores diferencias con respecto a la población general, con el cuestionario EQ-SD. Con el instrumento RAND-36, se obtuvieron algunas diferencias en las dimensiones de la esfera psicológica y funcionamiento social. Los pacientes con fatiga y disnea asociadas presentaron peores índices de calidad de vida a los 8 meses, con respecto a los que presentaban fatiga o disnea aisladas, o ninguna de ellas. No se observaron diferencias en los niveles de hemoglobina, proteína C reactiva o anticuerpos para SARS-CoV-2. La prueba de distancia de caminata de 6 minutos mostró diferencias significativas en los que presentaron fatiga por criterios de Fukuda (ver Cuadro 5). Las pruebas de función pulmonar fueron prácticamente normales a los 8 meses. Se realizó Rx de tórax a los 8 meses en los que presentaban disnea, y se encontraron alteraciones leves solo en el 7%2. Se aplicaron 4 pruebas cognitivas después de un año de la infección, con foco en la memoria y en la atención, que solo mostraron alteraciones leves.4 Como predictores de fatiga a los 30 meses se encontraron el haber presentado mayor cantidad de síntomas en la etapa aguda y puntajes más altos de ansiedad/depresión a los 3 meses. Los puntajes de disnea a los 30 meses fueron significativamente más altos en los que cumplieron los criterios de fatiga de Fukuda.
Conclusiones
• La prevalencia de fatiga fue alta en todos los puntos del estudio, con leve reducción en el tiempo.
• Las medidas objetivas, como las pruebas de función pulmonar, distancia de 6 minutos de caminata o pruebas de laboratorio, mostraron poca asociación con la fatiga a los 8 meses.
• Los criterios de Fukuda se asociaron con la distancia de caminata a los 6 minutos.
Referencias
1. Stavem K, et al. Persistent symptoms 1.5–6 months after COVID-19 in non-hospitalised subjects: a population-based cohort study. Thorax 2021;76(4):405-407.
2. Knut Stavem. Physiological and patient-reported outcomes over two years after COVID-19. April 17, 2023. Data no publicada presentada en el ECCMID 2023.
3. Fukuda K et al. The chronic fatigue syndrome: a comprehensive approach to its definition and study. International Chronic Fatigue Syndrome Study Group. Ann Intern Med 1994; 121(12): 953-9.
4. Stavem K, et al. Cognitive function in non-hospitalized patients 8–13 months after acute COVID-19 infection: A cohort study in Norway. PLoS ONE 2022; 17(8): e0273352.